Tìm kiếm phương trình hóa học
Hãy nhập vào chất tham gia hoặc/và chất sản phẩm để bắt đầu tìm kiếm
2CO + SO2 → S + 2CO2 | Cân Bằng Phương Trình Hóa Học
CO | cacbon oxit | Chất khí + SO2 | lưu hùynh dioxit | = S | sulfua | chất rắn + CO2 | Cacbon dioxit | Chất khí, Điều kiện Nhiệt độ 500, CO tác dụng với SO2.
Giới thiệu
Thông tin chi tiết về phương trình
Điều kiện phản ứng khi cho tác dụng CO + SO2
- Chất xúc tác: không có
- Nhiệt độ: 500
- Áp suất: thường
- Điều kiện khác: không có
Quá trình phản ứng CO + SO2
Quá trình: CO tác dụng với SO2.
Lưu ý: không có
Hiện tượng xảy ra sau phản ứng CO + SO2
Hiện tượng: đang cập nhật...
Thông tin chi tiết các chất tham gia phản ứng
Thông tin về CO (cacbon oxit)
- Nguyên tử khối: 28.0101
- Màu sắc: không màu, không mùi
- Trạng thái: Chất khí
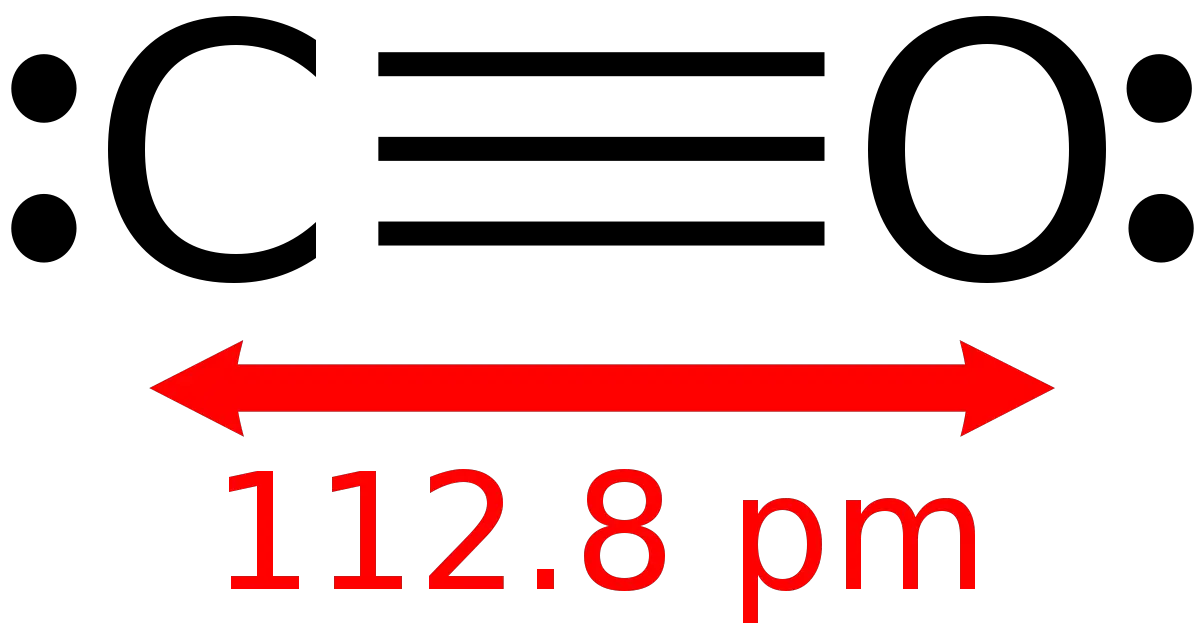
Cacbon monoxit, công thức hóa học là CO, là một chất khí không màu, không mùi, bắt cháy và có độc tính cao. Nó là sản phẩm chính trong sự cháy không hoàn toàn của cacbon và các hợp chất chứa cacbon. Có nhiều nguồn sinh ra cacbon monoxit. Khí thải của động cơ đốt trong tạo ra sau khi đốt các nhiên...
Thông tin về SO2 (lưu hùynh dioxit)
- Nguyên tử khối: 64.0638
- Màu sắc: chưa cập nhật
- Trạng thái: chưa cập nhật
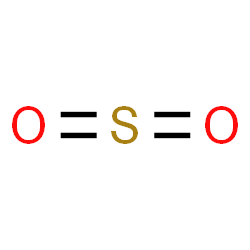
Sản xuất axit sunfuric(Ứng dụng quan trọng nhất) Tẩy trắng giấy, bột giấy, tẩy màu dung dịch đường Đôi khi được dùng làm chất bảo quản cho các loại quả sấy khô như mơ, vả v.v., do thuộc tính chống nấm mốc, và nó được gọi là E220 khi sử dụng vào việc này ở châu Âu. Với công dụng là một chất bảo qu...
Thông tin chi tiết các chất sản phẩm sau phản ứng
Thông tin về S (sulfua)
- Nguyên tử khối: 32.0650
- Màu sắc: vàng chanh
- Trạng thái: chất rắn
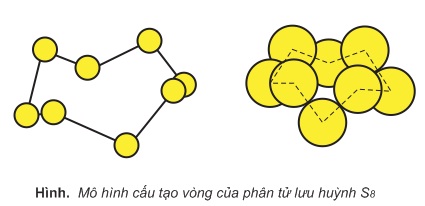
Lưu huỳnh có nhiều ứng dụng công nghiệp. Thông qua dẫn xuất chính của nó là axít sulfuric (H2SO4), lưu huỳnh được đánh giá là một trong các nguyên tố quan trọng nhất được sử dụng như là nguyên liệu công nghiệp. Nó là quan trọng bậc nhất đối với mọi lĩnh vực của nền kinh tế thế giới. Sản xuất axít...
Thông tin về CO2 (Cacbon dioxit)
- Nguyên tử khối: 44.0095
- Màu sắc: không màu, không mùi
- Trạng thái: Chất khí
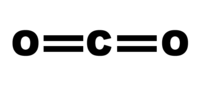
Carbon dioxide được sử dụng trong ngành công nghiệp thực phẩm, công nghiệp dầu mỏ và công nghiệp hóa chất. Hợp chất này có nhiều mục đích sử dụng thương mại khác nhau nhưng một trong những ứng dụng lớn nhất của nó như một chất hóa học là trong sản xuất đồ uống có ga; nó cung cấp sự lấp lánh trong đồ...
Tổng số đánh giá:
Xếp hạng: / 5 sao
Các phương trình điều chế CO
Chất xúc tác
thường
Nhiệt độ
thường
Áp suất
thường
Điều kiện khác
thường
Chất xúc tác
thường
Nhiệt độ
800 - 850
Áp suất
thường
Điều kiện khác
thường
Chất xúc tác
thường
Nhiệt độ
1200
Áp suất
thường
Điều kiện khác
thường
Các phương trình điều chế SO2
Chất xúc tác
thường
Nhiệt độ
thường
Áp suất
thường
Điều kiện khác
thường
Chất xúc tác
thường
Nhiệt độ
when heated
Áp suất
thường
Điều kiện khác
thường
Chất xúc tác
thường
Nhiệt độ
thường
Áp suất
thường
Điều kiện khác
thường
Một số định nghĩa cơ bản trong hoá học.
Mol là gì?
Trong hóa học, khái niệm mol được dùng để đo lượng chất có chứa 6,022.10²³ số hạt đơn vị nguyên tử hoặc phân tử chất đó. Số 6,02214129×10²³ - được gọi là hằng số Avogadro.
Xem thêmĐộ âm điện là gì?
Độ âm điện là đại lượng đặc trưng định lượng cho khả năng của một nguyên tử trong phân tử hút electron (liên kết) về phía mình.
Xem thêmKim loại là gì?
Kim loại (tiếng Hy Lạp là metallon) là nguyên tố có thể tạo ra các ion dương (cation) và có các liên kết kim loại, và đôi khi người ta cho rằng nó tương tự như là cation trong đám mây các điện tử.
Xem thêmNguyên tử là gì?
Nguyên tử là hạt nhỏ nhất của nguyên tố hóa học không thể chia nhỏ hơn được nữa về mặt hóa học.
Xem thêmPhi kim là gì?
Phi kim là những nguyên tố hóa học dễ nhận electron; ngoại trừ hiđrô, phi kim nằm bên phải bảng tuần hoàn.
Xem thêmNhững sự thật thú vị về hoá học có thể bạn chưa biết
Sự thật thú vị về Hidro
Hydro là nguyên tố đầu tiên trong bảng tuần hoàn. Nó là nguyên tử đơn giản nhất có thể bao gồm một proton trong hạt nhân được quay quanh bởi một electron duy nhất. Hydro là nguyên tố nhẹ nhất trong số các nguyên tố và là nguyên tố phong phú nhất trong vũ trụ.
Xem thêmSự thật thú vị về heli
Heli là một mặt hàng công nghiệp có nhiều công dụng quan trọng hơn bong bóng tiệc tùng và khiến giọng nói của bạn trở nên vui nhộn. Việc sử dụng nó là rất cần thiết trong y học, khí đốt cho máy bay, tên lửa điều áp và các tàu vũ trụ khác, nghiên cứu đông lạnh, laser, túi khí xe cộ, và làm chất làm mát cho lò phản ứng hạt nhân và nam châm siêu dẫn trong máy quét MRI. Các đặc tính của heli khiến nó trở nên không thể thiếu và trong nhiều trường hợp không có chất nào thay thế được heli.
Xem thêmSự thật thú vị về Lithium
Lithium là kim loại kiềm rất hoạt động về mặt hóa học, là kim loại mềm nhất. Lithium là một trong ba nguyên tố được tạo ra trong BigBang! Dưới đây là 20 sự thật thú vị về nguyên tố Lithium - một kim loại tuyệt vời!
Xem thêmSự thật thú vị về Berili
Berili (Be) có số nguyên tử là 4 và 4 proton trong hạt nhân của nó, nhưng nó cực kỳ hiếm cả trên Trái đất và trong vũ trụ. Kim loại kiềm thổ này chỉ xảy ra tự nhiên với các nguyên tố khác trong các hợp chất.
Xem thêmSự thật thú vị về Boron
Boron là nguyên tố thứ năm của bảng tuần hoàn, là một nguyên tố bán kim loại màu đen. Các hợp chất của nó đã được sử dụng hàng nghìn năm, nhưng bản thân nguyên tố này vẫn chưa bị cô lập cho đến đầu thế kỉ XIX.
Xem thêmSo sánh các chất hoá học phổ biến.
ErI3 và Al2(CO3)3
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Erbi triiodua và chất Nhôm cacbonat
Xem thêmBaSiO3 và Cu(BrO3)2.6H2O
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Bari metasilicat và chất Đồng(II) bromat hexahidrat
Xem thêmFe2SiO4 và O2PtF6
Điểm khác nhau về tính chất vật lý, hoá học giữa chất sắt(II) orthosilicat và chất Dioxygenyl hexafluoroplatinate
Xem thêmHfO2.nH2O và C2H5I
Điểm khác nhau về tính chất vật lý, hoá học giữa chất Hafni dioxit hidrat và chất Ety I-ot dua
Xem thêm


