I. TÍNH CHẤT VẬT LÍ
- Clo là chất khí, màu vàng lục, mùi hắc. Clo nặng gấp 2,5 lần không khí và tan được trong nước. Clo là khí độc.

II. TÍNH CHẤT HÓA HỌC
1. Clo có những tính chất hóa học của phi kim không?
a) Tác dụng với kim loại
Cl2(k) + Fe(r) ->2FeCl3(r) (điều kiện nhiệt độ)
Cl2(k) + Cu(r) -> CuCl2(r) (điều kiện nhiệt độ)
Kết luận: Clo tác dụng với hầu hết các kim loại tạo thành muối clorua.
b) Tác dụng với hiđro
Cl2(k) + H2(k) -> 2HCl(k) (điều kiện nhiệt độ)
-Khí HCl tan nhiều trong nước tạo thành dung dịch axit clohiđric.
Kết luận: Clo có những tính chất hóa học của phi kim. Clo là một phi kim hoạt động hóa học mạnh, clo không trực tiếp phản ứng với oxi.
2. Clo còn có những tính chất hóa học nào khác?
a) Tác dụng với nước
Cl2(k) + H2O(l) ⇌ HCl(dd) + HClO(dd) (phản ứng này xẩy ra theo hai chiều; phản ứng này được gọi là phản ứng thuận nghịch)
- Nước clo là dung dịch hỗn hợp các chất HCl, HClO và Cl2 nên có màu vàng lục, mùi hắc của khí clo. Nếu cho quì tím vào dd đó, lúc đầu quì tím hóa đỏ, sau đó nhanh chóng bị mất màu là do tác dụng oxi hóa mạnh của axit hipoclorơ HClO.
b) Tác dụng với dung dịch NaOH
Cl2(k) + 2NaOH(dd) → NaCl(dd) + NaClO(dd) + H2O
- Dung dịch hỗn hợp gồm NaCl (natri clorua) và NaClO (natri hipoclorit) được gọi là nước Gia-ven. Dung dịch này có tính tẩy màu vì tương tự như HClO, NaClO có tính oxi hóa mạnh.
III. ỨNG DỤNG CỦA CLO
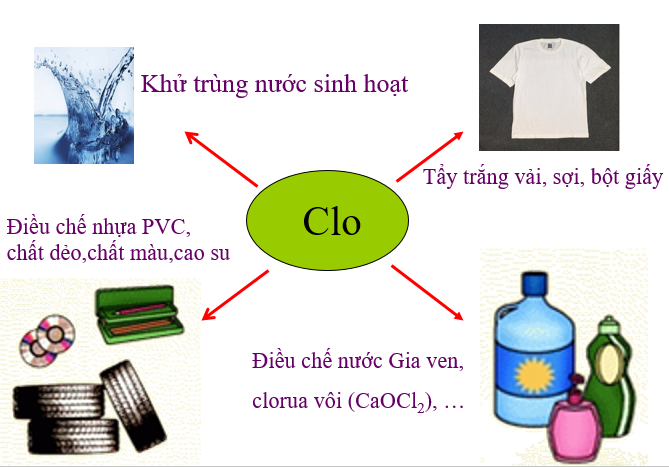
IV. ĐIỀU CHẾ KHÍ CLO
1.Điều chế trong phòng thí nghiệm
.png)
- Trong phòng thí nghiệm khí clo được điều chế bằng cách cho axit HCl đặc tác dụng với chất oxi hóa mạnh như MnO2 hoặc KMnO4.
4HCl(dd đặc) + MnO2(r) -> MnCl2(dd) + Cl2(k) + 2H2O (điều kiện nhiệt độ )
2. Điều chế trong công nghiệp
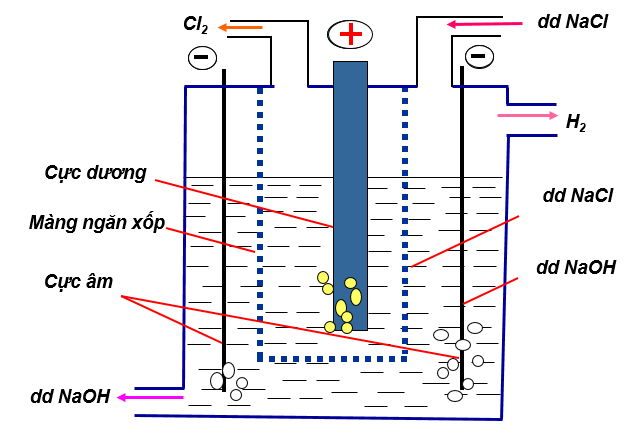
-Khí clo được điều chế bằng phương pháp điện phân dung dịch bão hòa NaCl, có màng ngăn xốp
2NaCl(dd) + 2H2O(l) -> 2NaOH(dd) + H2(k) + Cl2(k) (điều kiện nhiệt độ )
-Khí clo được chiều chế theo phương pháp này thường bị lẫn hơi ẩm. Để làm khô khí clo người ta dẫn khí clo qua dung dịch H2SO4 đặc 98% để làm khô. (Vì H2SO4 đặc có tính háo nước nên nó sẽ hập thụ hơi nước chứa trong khí clo)