I. THÀNH PHẦN CẤU TẠO CỦA NGUYÊN TỬ
1. Electron
a) Sự tìm ra electron
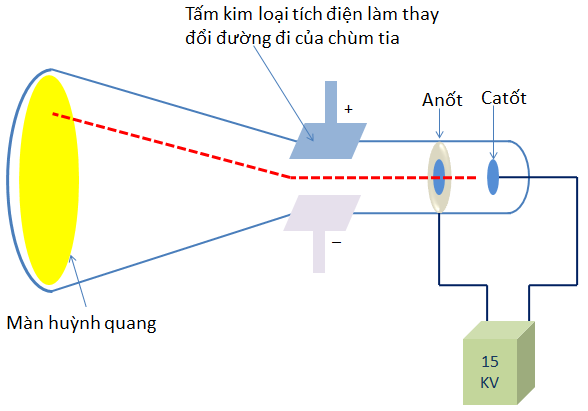
Năm 1897, nhà bác học người Anh Tôm-xơn (J.J. Thomson) nghiên cứu sự phóng điện giữa hai điện cực có hiệu điện thế 15kV, đặt trong một ống gần như chân không và thấy màn huỳnh quang trong ống phát sáng do những tia phát ra từ cực âm và được gọi là tia âm cực.
Người ta gọi những hạt tạo thành tia âm cực là các electron, kí hiệu là e.
b) Khối lượng và điện tích của electron
Khối lượng: me = 9,1094.10-31 kg.
Điện tích: qe = -1,602.10-19 C (culông).
2. Sự tìm ra hạt nhân nguyên tử
Năm 1911, nhà vật lí người Anh Rơ-dơ-pho và các cộng sự đã khám phá ra hạt nhân nguyên tử. Ông cho rằng nguyên tử có cấu tạo rỗng, phần mang điện dương là hạt nhân. Xung quanh hạt nhân có các electron tạo nên vỏ nguyên tử. Khối lượng nguyên tử hầu như tập trung ở hạt nhân.
3. Cấu tạo của hạt nhân nguyên tử
a) Sự tìm ra proton
Năm 1918, Rơ-dơ-pho đã tìm ra hạt proton khi bắn phá hạt nhân nguyên tử nitơ bằng hạt alpha. Hạt proton kí hiệu là chữ p. Hạt proton là một thành phần cấu tạo của hạt nhân nguyên tử.
b) Sự tìm ra nơtron
Năm 1932, Chat-uých dùng hạt alpha bắn phá hạt nhân nguyên tử beri đã phát hiện ra hạt nơtron (kí hiệu là n). Nơtron cũng là một thành phần cấu tạo của hạt nhân nguyên tử.
c) Cấu tạo của hạt nhân nguyên tử
Hạt nhân nguyên tử được tạo thành bởi các proton và nơtron. Vì nơtron không mang điện, số proton trong hạt nhân phải bằng số đơn vị điện tích dương của hạt nhân và bằng số electron quay xung quanh hạt nhân.
II. KÍCH THƯỚC VÀ KHỐI LƯỢNG CỦA NGUYÊN TỬ
1. Kích thước
Nguyên tử giống như một quả cầu, các electron chuyển động rất nhanh xung quanh hạt nhân, có đường kính khoảng 10-10 m.
a) Nguyên tử nhỏ nhất là nguyên tử H có bán kính khoảng 0,053 nm.
b) Đường kính của hạt nhân nguyên tử còn nhỏ hơn, vào khoảng 10-5 nm.
Đường kính của nguyên tử lớn hơn đường kính của hạt nhân cỡ 104 lần.
c) Đường kính của electron và của proton còn nhỏ hơn nhiều (khoảng 10-8 nm), electron chuyển động xung quanh hạt nhân trong không gian rỗng của nguyên tử.
2. Khối lượng
1 gam của bất kỳ chất nào cũng chứa hàng tỉ nguyên tử. Ví dụ: 1g cacbon có tới 5.1022 nguyên tử cacbon.
Để biểu thị khối lượng của nguyên tử, phân tử và các hạt proton, notron, electron, người ta phải dùng đơn vị khối lượng nguyên tử, kí hiệu u (hay còn gọi là đơn vị cacbon, đvC).
1u = 1/12 khối lượng của một nguyên tử đồng vị cacon 12; 1u = 1,66605.10-27 kg.
Khối lượng của 1 nguyên tử H = 1u, nguyên tử C = 12u, ...
me = 9,1094.10-31 kg = 0,00055u; mp = 1,6726.10-27 kg = 1u; mn = 1,6748.10-27 kg = 1u.
