I- NƯỚC LÀ CHẤT ĐIỆN LI RẤT YẾU
1. Sự điện li của nước
Bằng dụng cụ đo nhạy, người ta thấy nước cũng dẫn điện nhưng cực kì yếu.
Nước là chất điện li rất yếu: H2O ⇌ H+ + OH−(1)
2. Tích số ion của nước
Từ phương trình (1) ta có thể viết được biểu thức hằng số cân bằng K của phản ứng:
K=[H+][OH−] / [H2O]
Thực nghiệm đã xác định được rằng, ở nhiệt độ thường cứ 555 triệu phân tử nước chỉ có một phân tử phân li ra ion, nên [H2O] được coi là hằng số. Từ đó, đặt:
KH2O=K[H2O]=[H+].[OH−]
KH2O được coi là tích số ion của nước, tích số này là hằng số ở nhiệt độ xác định.
Ở 25oC:KH2O=[H+].[OH−]=1,0.10−14, tuy nhiên giá trị này còn được dùng ở nhiệt độ không khác nhiều với 25oC
Một cách gần đúng, có thể coi giá trị tích số ion của nước là hằng số cả trong dung dịch loãng của các chất khác nhau.
Vì một phân tử H2O phân li ra một ion H+ và một ion OH−, nên trong nước:
[H+]=[OH−]= √1,0.10−14=1,0.10−7M
Nước có môi trường trung tính, nên có thể định nghĩa:
Môi trường trung tính là môi trường trong đó [H+]=[OH−]=1,0.10−7M
3. Ý nghĩa tích số ion của nước
a) Môi trường axit
Khi hòa tan axit vào nước, nồng độ H+ tăng, nên nồng độ OH− phải giảm sao cho tích số ion của nước không đổi.
Thí dụ, hòa tan axit vào nước để nồng độ H+ bằng 1,0.10−3M thì nồng độ OH− là:
[OH−]=1,0.10−14 / [H+]=1,0.10−14 / 1,0.10−3=1,0.10−11M
Vậy môi trường axit là môi trường trong đó [H+]>[OH−] hay [H+]>1,0.10−7M.
b) Môi trường kiềm
Khi hòa tan bazơ vào nước, nồng độ OH− tăng, nên nồng độ H+ phải giảm sao cho tích số ion của nước không đổi. Thí dụ, hòa tan bazơ vào nước để nồng độ OH− bằng 1,0.10−5M thì nồng độ H+ là:
[H+]=1,0.10−14 / [OH−]=1,0.10−14 / 1,0.10−5=1,0.10−9M
Vậy môi trường kiềm là môi trường trong đó: [H+]<[OH−] hay [H+]<1,0.10−7M
Những thí dụ trên cho thấy, nếu biết nồng độ H+ trong dung dịch nước, thì nồng độ OH− cũng được xác định và ngược lại. Vì vậy, độ axit và độ kiềm của dung dịch có thể được đánh giá chỉ bằng nồng độ H+:
Môi trường trung tính: [H+]=1,0.10−7M
Môi trường axit: [H+]>1,0.10−7M
Môi trường kiềm: [H+]<1,0.10−7M
II - KHÁI NIỆM VỀ pH. CHẤT CHỈ THỊ AXIT - BAZƠ
1. Khái niệm về pH
Như đã thấy ở trên, dựa vào nồng độ H+ trong dung dịch nước có thể đánh giá được độ axit và độ kiềm của dung dịch. Nhưng dung dịch thường dùng có nồng độ H+ nhỏ, để tránh ghi nồng độ H+ với số mũ âm, người ta dùng pH với quy ước như sau:
[H+]=1,0.10−pH(∗)M. Nếu [H+]=1,0.10−aM thì pH=a.
Thí dụ: [H+]=1,0.10−1M⇒pH=1,00: môi trường axit.
[H+]=1,0.10−7M⇒pH=7,00: môi trường trung tính.
[H+]=1,0.10−11M⇒pH=11,00; môi trường kiềm.
Thang pH thường dùng có giá trị 1 đến 14.
Giá trị pH có ý nghĩa to lớn trong thực tế. Chẳng hạn, pH của máu người và động vật có giá trị gần như không đổi. Thực vật có thể sinh trưởng bình thường chỉ khi giá trị pH của dung dịch trong đất ở trong khoảng xác định đặc trưng cho mỗi loại cây. Tốc độ ăn mòn kim loại trong nước tự nhiên phụ thuộc rất nhiều vào pH của nước mà kim loại tiếp xúc.
2. Chất chỉ thị axit - bazơ
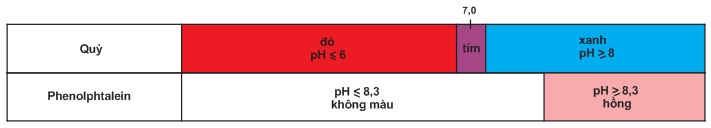
Chất chỉ thị axit - bazơ là chất có màu biến đổi phụ thuộc vào giá trị pH của dung dịch. Thí dụ, màu của hai chất chỉ thị axit bazơ là quỳ và phenolphtalein trong các khoảng pH khác nhau được đưa ra trong bảng 1.1.
Bảng 1.1. Màu của quỳ và phenolphtalein trong dung dịch ở các khoảng pH khác nhau.
Trộn lẫn một số chất chỉ thị có màu biến đổi kế tiếp nhau theo giá trị pH, ta được hỗn hợp chất chỉ thị vạn năng. Dùng băng giấy tẩm dung dịch hỗn hợp này có thể xác định được gần đúng giá trị pH của dung dịch
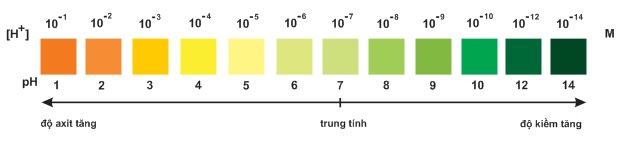
Hình Màu của chất chỉ thị vạn năng (thuốc thử MERCK của Đức) ở các giá trị pH khác nhau.
Để xác định tương đối chính xác giá trị pH của dung dịch người ta dùng máy đo pH.