I- THUYẾT CẤU TẠO HÓA HỌC
1. Nội dung của thuyết cấu tạo hóa học
Ngay từ năm 1861, Bút-lê-rốp đã đưa ra khái niệm cấu tạo hóa học và thuyết cấu tạo hóa học gồm những luận điểm chính sau:
1. Trong phân tử hợp chất hữu cơ, các nguyên tử liên kết với nhau theo đúng hóa trị và theo một thứ tự nhất định. Thứ tự liên kết đó được gọi là cấu tạo hóa học. Sự thay đổi thứ tự liên kết đó, tức là thay đổi cấu tạo hóa học, sẽ tạo ra hợp chất khác.
Thí dụ: Công thức phân tử C2H6O có hai công thức cấu tạo (thứ tự liên kết khác nhau) ứng với 2 hợp chất sau:
H3C−O−CH3: đimetyl ete, chất khí, không tác dụng với Na.
H3C−CH2−O−H: ancol etylic, chất lỏng, tác dụng với Na giải phóng hiđro.
2. Trong phân tử hợp chất hữu cơ, cacbon có hóa trị 4. Nguyên tử cacbon không những có thể liên kết với nguyên tử các nguyên tố khác mà còn liên kết với nhau thành mạch cacbon.
Thí dụ:
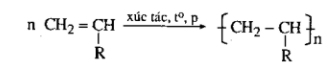
3. Tính chất của các chất phụ thuộc vào thành phần phân tử (bản chất, số lượng các nguyên tử) và cấu tạo hóa học (thứ tự liên kết các nguyên tử).
Thí dụ:
- Phụ thuộc thành phần phân tử: CH4 là chất khí dễ cháy, CCl4 là chất lỏng không cháy; CH3Cl là chất khí không có tác dụng gây mê, còn CHCl3 là chất lỏng có tác dụng gây mê.
- Phụ thuộc cấu tạo hóa học: CH3CH2OH và CH3OCH3 khác nhau cả về tính chất hóa học.
2. Đồng đẳng, đồng phân
a) Đồng đẳng
Các hiđrocacbon trong dãy: CH4,C2H6,C3H8,C4H10,C5H12,...,CnH2n+2, chất sau hơn chất trước một nhóm CH2 nhưng đều có tính chất hóa học tương tự nhau.
Các ancol trong dãy: CH3OH,C2H5OH,C3H7OH,C4H9OH,...,CnH2n+1OH cũng có thành phần hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hóa học tương tự nhau.
* Khái niệm: Những hợp chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hóa học tương tự nhau là những chất đồng đẳng, chúng hợp thành dãy đồng đẳng.
* Giải thích: Mặc dù các chất trong cùng dãy đồng đẳng có công thức phân tử khác nhau một hay nhiều nhóm CH2 nhưng do chúng có cấu tạo hóa học tương tự nhau nên có tính chất hóa học tương tự nhau.
b) Đồng phân
Etanol và đimetyl ete là hai chất khác nhau (có tính chất khác nhau ) nhưng có cùng công thức phân tử là C2H6O.
Metyl axetat (CH3COOCH3), etyl fomiat (HCOOC2H5) và axit propionic (CH3CH2COOH) là ba chất khác nhau nhưng có công thức phân tử là C3H6O2.
* Khái niệm: Những hợp chất khác nhau nhưng có cùng công thức phân tử là những chất đồng phân.
* Giải thích: Những chất đồng phân tuy có cùng công thức phân tử nhưng có cấu tạo hóa học khác nhau, chẳng hạn etanol có cấu tạo H3C−CH2−O−H, còn đimetyl ete có cấu tạo H3C−O−CH3, vì vậy chúng là những chất khác nhau, có tính chất khác nhau.
II - LIÊN KẾT TRONG PHÂN TỬ HỢP CHẤT HỮU CƠ
1. Các loại liên kết trong phân tử hợp chất hữu cơ
Theo Li-uýt (Lewis), các nguyên tử có xu hướng dùng chung electron để đạt được 8 electron (đối với Hchỉ cần đạt 2 electron) ở lớp ngoài cùng (quy tắc bát tử).
Công thức có viết đầy đủ các electron hóa trị được gọi là công thức Li-uýt.
Thí dụ:
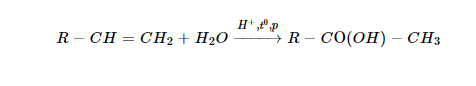
Liên kết trong phân tử các hợp chất hữu cơ chủ yếu dựa vào sự dùng chung các cặp elctron (liên kết cộng hóa trị)
* Liên kết tạo bởi 1 cặp electron dùng chung là liên kết đơn được biểu diễn bởi 2 dấu chấm hay 1 gạch nối giữa 2 nguyên tử.
* Liên kết tạo bởi 2 cặp electron dùng chung là liên kết đôi. Liên kết đôi gồm 1 liên kết σ và 1 liên kết π, biểu diễn bởi 4 dấu chấm hay 3 gạch nối.
* Liên kết tạo bởi 3 cặp electron dùng chung là liên kết ba. Liên kết ba gồm 1 liên kết σ và 2 liên kết π, biểu diễn bởi 6 chấm hay 3 gạch nối.
* Liên kết đôi và liên kết ba gọi chung là liên kết bội.
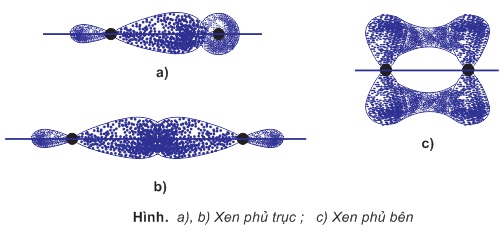
Nguyên tử C sử dụng obitan lai hóa để tạo liên kết σ theo kiểu xen phủ trục (hình a,b) và dùng obitan p để tạo liên kết π theo kiểu xen phủ bên (hình c).
2. Các loại công thức cấu tạo
Công thức cấu tạo biểu diễn thứ tự và cách thức liên kết của các nguyên tử trong phân tử. Có cách viết khai triển, thu gọn và thu gọn nhất.
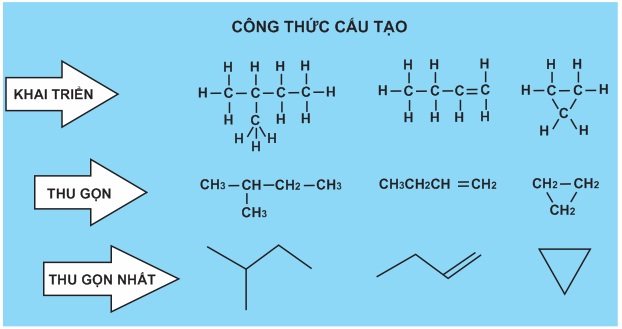
Công thức cấu tạo khai triển: Viết tất cả các nguyên tử và các liên kết giữa chúng.
Công thức cấu tạo thu gọn: Viết gộp nguyên tử cacbon và các nguyên tử khác liên kết với nó thành từng nhóm.
Công thức cấu tạo thu gọn nhất: Chỉ viết các liên kết và nhóm chức, đầu mút của các liên kết chính là nhóm CHx với x đảm bảo hóa trị 4 ở C.
III - ĐỒNG PHÂN CẤU TẠO
1. Khái niệm đồng phân cấu tạo
a) Thí dụ
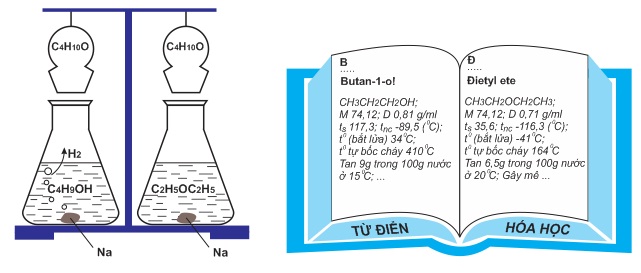
b) Kết luận
Butan−1−ol và đietylete có cùng công thức phân tử C4H10O nhưng do khác nhau về cấu tạo hóa học nên khác nhau về tính chất vật lí và tính chất hóa học.
Vậy những hợp chất có cùng công thức phân tử nhưng có cấu tạo hóa học khác nhau gọi là những đồng phân cấu tạo.
2. Phân loại đồng phân cấu tạo
a) Thí dụ:
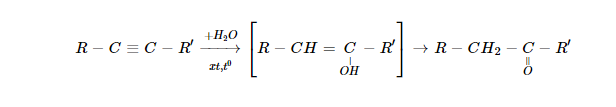
b) Kết luận
Những đồng phân khác nhau về bản chất nhóm chức gọi là đồng phân nhóm chức. Những đồng phân khác nhau về sự phân nhánh mạch cacbon gọi là đồng phân mạch cacbon. Những đồng phân khác nhau về vị trí nhóm chức gọi là đồng phân vị trí nhóm chức.
IV- CÁCH BIỂU DIỄN CẤU TRÚC KHÔNG GIAN PHÂN TỬ HỮU CƠ
1. Công thức phối cảnh
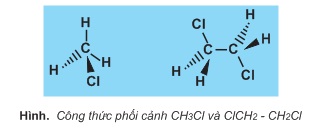
Công thức phối cảnh là một loại công thức lập thể.
Đường nét liền biểu diễn liên kết nằm trên mặt trang giấy.
Đường nét đậm biểu diễn liên kết hướng về mắt ta (ra phía trước trang giấy).
Đường nét đứt biểu diễn liên kết hướng ra xa mắt ta (ra phía sau trang giấy).
2. Mô hình phân tử
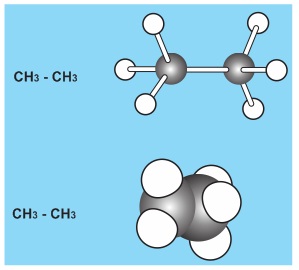
a) Mô hình rỗng
Các quả cầu tượng trưng cho các nguyên tử, các thanh nối tượng trưng cho các liên kết giữa chúng. Góc giữa hai các thanh nối bằng góc lai hóa.
b) Mô hình đặc
Các quả cầu cắt vát tượng trưng cho các nguyên tử được ghép với nhau theo đúng vị trí không gian của chúng.
V- ĐỒNG PHÂN LẬP THỂ
1. Khái niệm về đồng phân lập thể
a) Thí dụ
Ứng với công thức cấu tạo CHCl=CHCl có hai cách sắp xếp không gian khác nhau dẫn tới hai chất đồng phân:
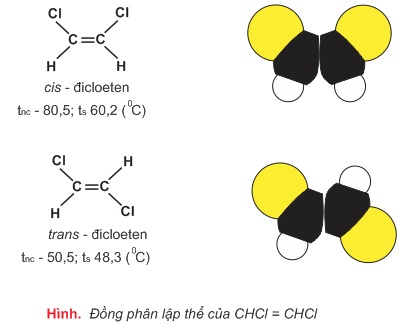
b) Kết luận
Đồng phân lập thể là những đồng phân có cấu tạo hóa học như sau (cùng công thức cấu tạo) nhưng khác nhau về sự phân bố không gian của các nguyên tử trong phân tử (tức khác nhau về cấu trúc không gian của phân tử)
2. Quan hệ giữa đồng phân cấu tạo và đồng phân lập thể

3. Cấu tạo hóa học và cấu trúc hóa học
Cấu tạo hóa học cho ta biết các nguyên tử liên kết với nhau theo thứ tự nào, bằng liên kết đơn hay liên kết bội, nhưng không cho biết sự phân bố trong không gian của chúng. Cấu tạo hóa học được biểu diễn bởi công thức cấu tạo.
Cấu tạo hóa học và cấu trúc không gian của phân tử hợp thành cấu trúc hóa học.
Cấu trúc hóa học vừa cho biết cấu tạo hóa học vừa cho biết sự phân bố trong không gian của các nguyên tử trong phân tử. Cấu trúc hóa học thường được biểu diễn bởi công thức lập thể.