Định luật bảo toàn khối lượng
Định luật bảo toàn khối lượng hay định luật Lomonosov - Lavoisier là một định luật cơ bản trong lĩnh vực hóa học, được phát biểu như sau: "Trong phản ứng hóa học, tổng khối lượng các chất tham gia phản ứng bằng tổng khối lượng các sản phẩm tạo thành".
Phương trình tổng quát: aA + bB cC + dD
Định luật BTKT: mA +mB = mC + mD
Ví dụ: 4,04g khí hidro kết hợp với đúng 32g khí oxi cho 36,04 g nước.
Theo lí thuyết nguyên tử, số lượng các nguyên tử của từng nguyên tố trước và sau phản ứng là như nhau, chỉ có sự sắp xếp lại các nguyên tử trong các phân tử tác chất thành các phân tử sản phẩm. Kết quả là tổng khối lượng các sản phẩm phải đúng bằng tổng khối lượng các chất ban đầu đã tác dụng.
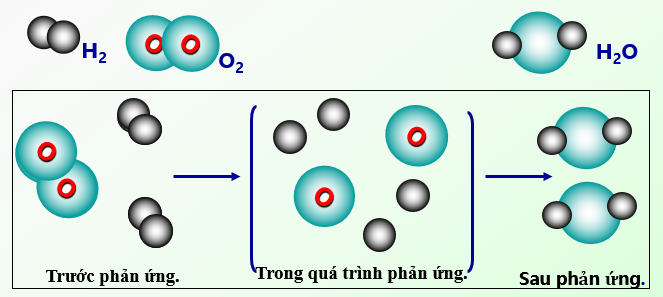
Ví dụ trên có thể minh họa bằng sơ đồ
Sử dụng phương trình hóa học ta có thể diễn đạt định luật bảo toàn khối lượng qua ví dụ trên như sau:
2H2 (k) + O2 (k) 2H2O (k)
hai phân tử + môt phân tử hai phân tử
2mol + 1mol 2 mol
2*2,02 = 4,04g + 32,00g 2+18,02 = 36,04g.
Theo vật lí học hiện đại, định luật bảo toàn khối lượng chỉ hoàn toàn chính xác khi các phản ứng hóa học không kèm theo hiệu ứng nhiệt. Trong trường hợp ngược lại, khi phản ứng hấp thụ (hoặc giải phóng) một năng lượng Q, khối lượng của hỗn hợp phản ứng phải tăng (hoặc giảm) một lượng thỏa mãn định luật Einstein
Tuy nhiên, do hiệu ứng nhiệt của các phản ứng hóa học chỉ vào khoảng 102 kcal.mol-1, ứng với sự thay đổi khối lượng khoảng:
= 0,465.10-11kg
Vì sự thay đổi khối lượng rất nhỏ, trong thực tế ngoài giới hạn của phép cân chính xác hiện thời, do vậy người ta vẫn thừa nhận định luật bảo toàn khối lượng.