1. Khái niệm, phân loại, danh pháp và đồng phân
a. Khái niệm và phân loại
Amin là dẫn xuất của amoniac, trong đó nguyên tử hidro được thay thế bằng gốc hidrocacbon (no, không no, thơm). Tùy theo số gốc hidrocacbon liên kết với nguyên tử nito mà có các loại amin bậc 1, bậc 2, bậc 3, muối amoni bậc 4.
RNH2 (Amin bậc 1) R2NH (Amin bậc 2) R3N ( Amin bậc 3) (Amoni bậc 4)
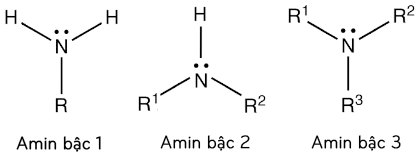
Tùy thuộc vào đặc điểm của gốc hidrocacbon mà ta có các loại amin tương ứng như amin thơm, amin mạch hở béo, amin không no...
b. Danh pháp
Tên của các amin được gọi theo danh pháp gốc - chức và danh pháp thay thế. Ngoài ra, một số amin được gọi theo tên thường (tên riêng) như ở bảng dưới. Nhóm NH2 khi đóng vai trò nhóm thế thì gọi là nhóm amino, khi đóng vai trò là nhóm chức chính thì gọi là amin.
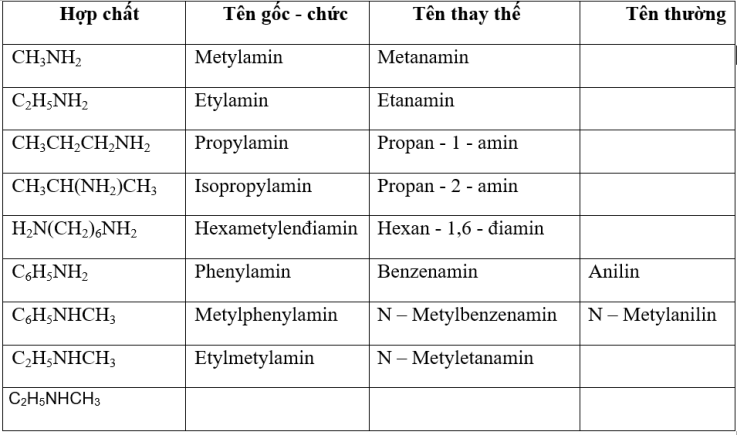
c. Đồng phân
Khi viết công thức các đồng phân cấu tạo của amin, cần viết đồng phân mạch cacbon và đồng phân vị trí nhóm chức cho từng loại: amin bậc I, amin bậc II, amin bậc III.
2. Tính chất vật lí
Các amin thấp là những chất khí, tan trong nước. Các đồng đẳng cao hơn là chất lỏng hoặc chất rắn và độ tan trong nước của chúng giảm dần. Các amin thấp có mùi khó chịu, gần giống như mùi amoniac. Các amin cao hoặc không mùi, hoặc có mùi rất yếu.
Các arylamin là chất lỏng, chất rắn không màu nhưng ở ngoài không khí chúng dần thẫm màu lại. Các arylamin có mùi khó chịu và rất độc. Tương tự ancol, các phân tử amin có thể kết hợp với nhau nhờ liên kết hidro, nhưng yếu hơn ở ancol rất nhiều do nitơ có độ âm điện kém hơn oxi.
Anilin là chất lỏng, sôi ở 184oC, không màu, rất độc, ít tan trong nước, tan trong etanol, benzen. Để lâu trong không khí, anilin chuyển sang màu nâu đen vì bị oxi hóa bởi không khí.
3. Cấu tạo phân tử và tính chất hóa học
Sự tương đồng về cấu tạo giữa amoniac, amin các bậc được thấy ở hình dưới đây.

Do phân tử amin có nguyên tử nito còn đôi electron chưa liên kết (tương tự phân tử amoniac) nên amin thể hiện tính bazơ, ngoài ra nitơ trong phân tử amin có số oxi hóa -3 như trong amoniac nên amin thường dễ bị oxi hóa. Các amin thơm, thí dụ anilin còn dễ dàng tham gia phản ứng thế vào nhân thơm do ảnh hưởng của đôi electron chưa liên kết ở nguyên tử nitơ.
a. Tính chất của chức amin
- Tính bazơ
+ Tác dụng với chất chỉ thị
+ Tác dụng với axit:
Dung dịch metylamin và nhiều đồng đẳng của nó có khả năng làm xanh giấy quỳ tím hoặc làm hồng phenolphtalein do kết hợp với proton mạnh hơn amoniac.
Anilin và các amin thơm rất ít tan trong nước. Dung dịch của nó không làm đổi màu quỳ tím và phenolphtalein.
Như vậy, nhóm ankyl có ảnh hưởng làm tăng mật độ electron ở nguyên tử nitơ do đó làm tăng lực bazơ; nhóm phenyl (-C6H5) làm giảm mật độ electron ở nguyên tử nitơ do đó làm giảm lực bazơ
Lực bazơ:
b. Phản ứng với axit nitrơ
Amin bậc một:
Amin bậc một dãy béo tác dụng với axit nitrơ tạo thành ancol tương ứng và giải phóng khí N2
C2H5-NH2 + HONO → C2H5-OH + N2 + H2O (xúc tác HCl)
Amin bậc một dãy thơm tác dụng với axit nitrơ (ở lạnh) tạo thành muối điazoni Ar-N(+)=NX(-)
C6H5-NH2 + HONO + HCl → C6H5-N=NCl (Benzenđiazoni clorua) + 2H2O
(Phản ứng xảy ra ở nhiệt độ 0 - 5oC)
Các muối điazoni chỉ bền trong dung dịch và ở nhiệt độ thấp. Khi đun nóng muối điazoni ở dạng khan sẽ nổ mạnh, nếu đun dung dịch nước của muối này sẽ tạo thành phenol và khí Nitơ.
C6H5-N=NCl + H2O → HCl + N2 + C6H5OH
Muối điazoni có khả năng phản ứng cao, được dùng nhiều trong tổng hợp hữu cơ nói chung và đặc biệt là tổng hợp các phẩm nhuộm chứa azo-N=N- trong phân tử gọi là phẩm azo.
Amin bậc hai:
Amin bậc hai dãy béo cũng như dãy thơm đều tác dụng với axit nitrơ sinh ra nitrosamin (nitrosoamin) là những chất màu vàng, nhờ đó phân biệt được amin bậc hai với amin bậc một:
(CH3)2N-H + HONO → (CH3)2N-N=O + H2O
C6H5-NH-CH3 + HONO → C6H5-N2O-CH3 + H2O
Amin bậc ba:
Amin bậc 3 dãy béo không tác dụng với axit nitrơ hoặc chỉ tạo thành muối không bền dễ bị thủy phân
Amin bậc 3 dãy thơm tác dụng với axit nitrơ cho sản phẩm thế ở nhân thơm.
Ví dụ:
(CH3)2N-C6H5 + HONO → p-(CH3)2N-C6H4-NO + H2O (xúc tác axit HCl)
c. Phản ứng thế gốc thơm
Các nhóm -NH2, -NHCH3... là những nhóm hoạt hóa nhân thơm và định hướng cho phản ứng thế xảy ra ở vị trí ortho và para.
Halogen hóa: Tương tự phenol, anilin tác dụng với nước brom tạo thành kết tủa trắng 2,4,6-tribromoanilin
Sunfo hóa: Đun nóng anilin với H2SO4 đậm đặc ở 180oC sẽ xảy ra một chuỗi phản ứng tạo thành sản phẩm cuối cùng là axit sunfanilic. Các amit của axit sunfanilic, gọi là sunfonamit hay sunfamit có tính sát trùng - kháng sinh, được dùng nhiều làm thuốc trị bệnh.
Ngoài ra Amin còn tham gia phản ứng thế nguyên tử hiđro của nhóm amino; gồm phản ứng ankyl hóa, phản ứng axyl hóa và phản ứng tạo thành isonitrin.
4. Ứng dụng và điều chế
a. Ứng dụng
Các ankylamin được dùng trong tổng hợp hữu cơ, đặc biệt là các điamin được dùng để tổng hợp polime.
Anilin là nguyên liệu quan trọng trong công nghiệp phẩm nhuộm (phẩm azo, đen anilin...), polime (nhựa anilin - fomadehit,..), dược phẩm (stretoxit, sunfaguanidin,..)
b. Điều chế
Amin có thể được điều chế bằng nhiều cách
- Ankyl hóa amoniac và amin bậc thấp hơn:
Dẫn xuất halogen tác dụng với amoniac và với amin tạo thành một hỗn hợp amin có bậc khác nhau và muối amoni bậc bốn. Nếu trong sơ đồ diều chế dùng dư amoniac, amin bậc một chiếm ưu thế. Điều chế riêng amin bậc một (không lẫn amin bậc cao hơn), người ta ankyl hóa kali phtalimit rồi thủy phân sản phẩm.
Khử hợp chất chứa nitro:
Có hai cách khử nitrobenzen trong công nghiệp:
Khử bằng khí hiđro có mặt chất xúc tác kim loại (Cu, Pt, Ni...):
C6H5-NO2 + 3H2 → C6H5-NH2 + 2H2O ΔH = -496kJ/mol
Khử bằng vỏ bào sắt, có mặt axit clohidric (sử dụng [H] mới sinh từ phản ứng Fe + HCl)
4C6H5-NO2 + 9Fe + 4H2O → 4C6H5-NH2 + 3Fe3O4
Nguy hiểm
Các ankyl amin và amin gốc hidrocacbon mạch thẳng là những hợp chất dễ bay hơi có mùi giống amoniac và rất độc. Chúng thường tồn tại trong các thịt cá và là nguyên nhân khiến thực phẩm có mùi tanh ôi. Do đó để khử bớt các amin người ta thường dùng giấm hoặc chanh.
Anilin và các amin vòng thơm là những chất lỏng hoặc rắn không tan trong nước khi dây vào da sẽ gây bỏng rát do đó phải hết sức cẩn thận khi tiếp xúc với anilin và các amin vòng thơm
